當(dāng)前位置:首頁(yè) > 新聞動(dòng)態(tài)
凱氏定氮儀原理及應(yīng)用
講凱氏定氮儀之前,我們先來(lái)認(rèn)識(shí)下蛋白質(zhì);蛋白質(zhì)是有機(jī)大分子,是生命活動(dòng)的主要承擔(dān)者。沒(méi)有蛋白質(zhì)就沒(méi)有生命。
蛋白質(zhì)是由氨基酸以“脫水縮合”的方式組成的多肽鏈經(jīng)過(guò)盤(pán)曲折疊形成的具有一定空間結(jié)構(gòu)的物質(zhì)。
一個(gè)氨基酸分子的羧基(-COOH)和另一個(gè)氨基酸分子的氨基(-NH2)相連接,同時(shí)脫去一分子水,形成肽鍵(-NH-CO-),這種方式叫做脫水縮合反應(yīng)。
凱氏定氮儀的由來(lái),丹麥化學(xué)家凱耶達(dá)爾(J. Kjeldahl)于1883年提出的濕法定量測(cè)定含氮有機(jī)化合物中氮的方法。
凱氏定氮法主要用來(lái)測(cè)定樣品中有機(jī)氮含量
有機(jī)物即有機(jī)化合物。含碳化合物(一氧化碳、二氧化碳、碳酸鹽、金屬碳化物等少數(shù)簡(jiǎn)單含碳化合物除外)或碳?xì)浠衔锛捌溲苌锏目偡Q。有機(jī)物是生命產(chǎn)生的物質(zhì)基礎(chǔ)。
有機(jī)化合物除少數(shù)以外,一般都能燃燒。和無(wú)機(jī)物相比,它們的熱穩(wěn)定性比較差,電解質(zhì)受熱容易分解。有機(jī)物的熔點(diǎn)較低,一般不超過(guò)400℃。
凱氏定氮儀測(cè)量樣品蛋白質(zhì)含量主要經(jīng)過(guò)三個(gè)步驟;
第一步:消解 目的是將有機(jī)物中的胺根在高溫和催化劑CuSO4,濃H2SO4 作用下反應(yīng),生成(NH4)2SO4
反應(yīng)方程式:
2NH2-+H2SO4+2H+=(NH4)2SO4
第二步 蒸餾 目的是將消解完成的樣品在凱氏定氮儀中與堿發(fā)生反應(yīng),通過(guò)蒸餾釋放出NH3 ;
反應(yīng)方程式:
(NH4)2SO4+2NaOH=2NH3+2H2O+Na2SO4
反應(yīng)完成后,用H3BO3 溶液收集蒸餾釋放出NH3,
反應(yīng)方程式:
2NH3+4H3BO3=(NH4)2B4O7+5H2O
第三步 滴定 目的是將收集的NH3通過(guò)已知含量的標(biāo)準(zhǔn)酸滴定,反算出NH3的含量;
反應(yīng)方程式:
(NH4)2B4O7+H2SO4+5H2O=(NH4)2SO4+4H3BO3
(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3
單位注解:
N:樣品中蛋白質(zhì)的百分含量;
V:樣品消耗硫酸或鹽酸標(biāo)準(zhǔn)液的體積,ml;
V空白:試劑空白消耗硫酸或鹽酸標(biāo)準(zhǔn)溶液的體積,ml;
C:硫酸或鹽酸標(biāo)準(zhǔn)溶液的當(dāng)量濃度
M:稱量樣品的重量,g;
氮含量計(jì)算公式:
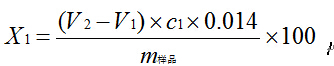
蛋白質(zhì)轉(zhuǎn)換系數(shù):
(1)一切蛋白質(zhì)都含N元素,且各種蛋白質(zhì)的含氮量很接近,平均為16%;
(2)蛋白質(zhì)系數(shù):任何生物樣品中每1g元N的存在,就表示大約有1/16%=6.25g蛋白質(zhì)的存在, 6.25常稱為蛋白質(zhì)常數(shù)
凱氏定氮儀的原理大致就是以上所述;那么凱氏定氮儀適合在什么環(huán)境下工作呢?需要一個(gè)正規(guī)的化學(xué)實(shí)驗(yàn)室
1、電源電壓:AC 220V±10% 50Hz;
2、自來(lái)水壓力:0.02MPa-1MPa;
3、環(huán)境溫度:室溫——35℃;
了解更多詳細(xì)內(nèi)容,推薦參考定氮儀視頻教程。

